臨床試驗既是醫學科學技術創新工作中的重要環節,又是確保醫學科學技術創新成果應用于臨床“安全、有效”的重要保證。為加強和規范國家醫療器械臨床試驗機構的管理,國家食品藥品監督管理總局發布《總局辦公廳關于做好醫療器械臨床試驗機構備案工作的通知》(食藥監辦械管〔2017〕161號),明確規定自2019年1月1日起,如果醫療機構未完成醫療器械臨床試驗機構備案工作,將不能承接注冊類醫療器械(包括體外診斷試劑)臨床試驗。
市一院藥物臨床試驗機構辦公室自2018年10月成立并成功通過國家藥品監督管理局認定,后又依規在國家藥物臨床試驗機構備案管理信息平臺完成備案工作。在充分總結醫院國家藥物臨床試驗機構創建、籌備經驗的基礎上,在院領導關心支持及相關科室的積極配合下,臨床試驗機構辦公室(機構辦)制定我院醫療器械專業評估細則,對醫院重點專學科進行認真的評估和篩選,6月初召開醫療器械臨床試驗機構備案啟動會,6-7月對申請器械備案的專業組在人員資質、文件制度、場地設施、培訓記錄等方面進行現場內部檢查評估。確認符合國家相關要求后,機構辦統一對通過內審評估的專業在國家藥監局備案系統進行了醫療器械臨床試驗機構與專業的信息備案。此次成功備案的科室包括眼科、口腔科、耳鼻咽喉科、腎內科、消化內科、醫學檢驗科6個科室共26個亞專業。
藥物臨床試驗機構、醫療器械臨床試驗機構的相繼依法依規成功備案,對醫療衛生機構科研隊伍建設、醫療技術質量、醫院社會聲譽的提高具有重要的意義。臨床試驗機構及臨床試驗專業,既是一所醫院醫療水平和科研能力的綜合體現,又是借助這些臨床試驗機構平臺,加強與國內外同行交流與合作的主要橋梁,更是有效培養醫院優質科研人才、提高醫院的綜合技術能力和專業特色優勢的重要平臺。市一院將繼續堅持依法、合規、有利和科技倫理原則釋放臨床資源,有效助推醫療器械研發與科技進步,促進和提升市一院社會影響力,更好的為人民群眾健康服務。機構辦將繼續嚴格遵守國家相關法律法規,進一步加強自身建設,管理服務好醫院的臨床試驗工作。
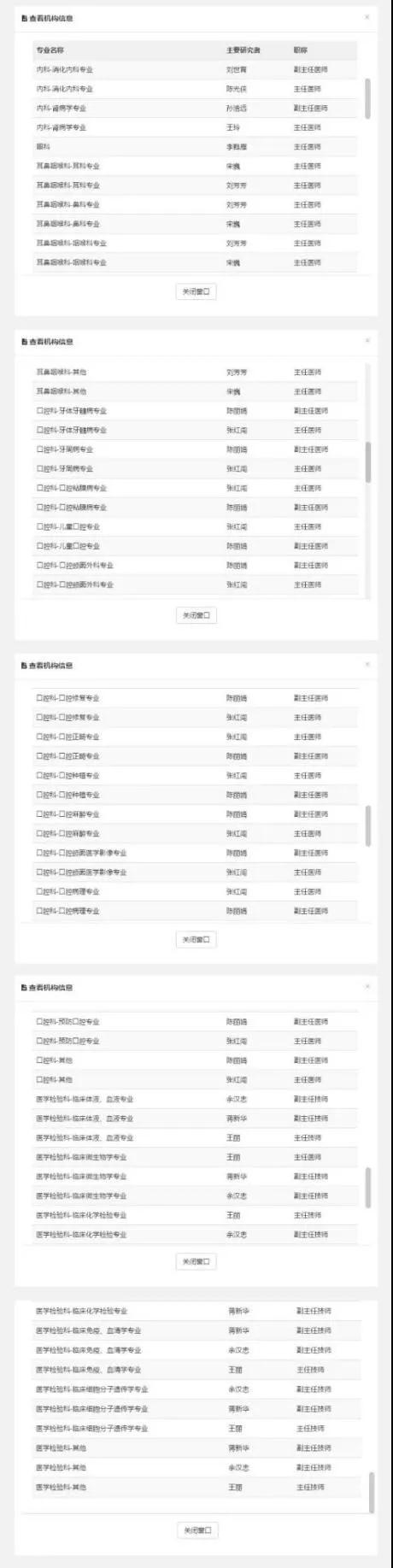
· 圖為醫療器械臨床試驗機構成功備案的6個科室和26個亞專業 ·
徐州健康熱線:0516-85707122









